국내 최초 임상·개발·허가·승인까지 독자 완성
일본 기술수출 및 아시아 임상 3상으로 글로벌 확장 가속화
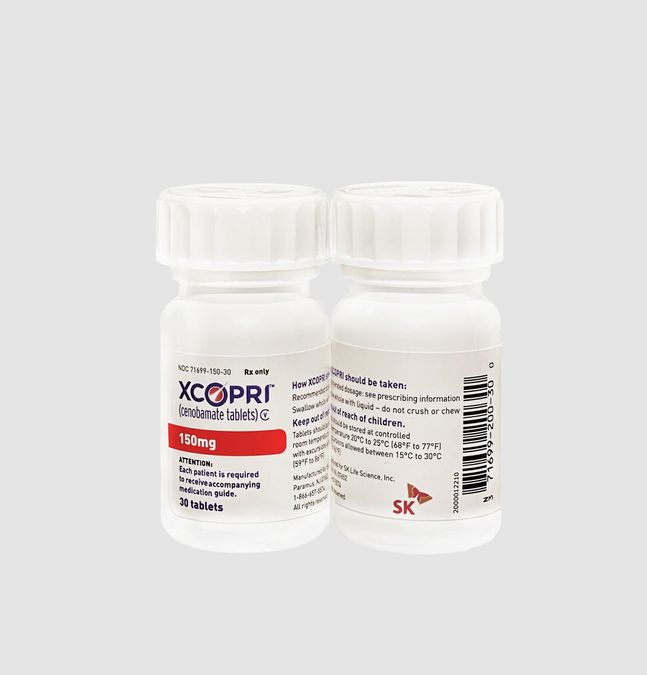 SK바이오팜은 후보물질 발굴부터 글로벌 임상개발, 인허가 및 시판까지 전 과정을 국내 최초로 독자 수행한 혁신신약 세노바메이트(제품명 엑스코프리)가 미국 FDA(식품의약국) 승인 1주년을 맞았다고 23일 밝혔다. ⓒSK바이오팜
SK바이오팜은 후보물질 발굴부터 글로벌 임상개발, 인허가 및 시판까지 전 과정을 국내 최초로 독자 수행한 혁신신약 세노바메이트(제품명 엑스코프리)가 미국 FDA(식품의약국) 승인 1주년을 맞았다고 23일 밝혔다. ⓒSK바이오팜
SK바이오팜은 후보물질 발굴부터 글로벌 임상개발, 인허가 및 시판까지 전 과정을 국내 최초로 독자 수행한 혁신신약 세노바메이트(제품명 엑스코프리)가 미국 FDA(식품의약국) 승인 1주년을 맞았다고 23일 밝혔다.
세노바메이트는 성인 대상 부분발작 치료제로, 임상시험에서 발작 빈도 감소율은 물론이고, 발작 완전 소실률(seizure freedom)에서도 통계적 유의성을 인정받았다.
약물 투약 기간 중에 발작이 발생하지 않는 발작 완전 소실은 환자의 일상이 정상으로 돌아간다는 것을 의미한다. 이는 삶의 질을 향상시킬 수 있는 가장 중요한 요소이며, 뇌전증 신약을 선택할 때 핵심적인 지표로 받아들여지고 있다.
조정우 SK바이오팜 사장은 "세노바메이트를 넘어 R&D 투자를 통해 신약을 지속적으로 창출해야 한다는 사명감을 갖고, 궁극적으로 사회적 가치의 지속 성장을 가능케 하는 글로벌 기업으로 발전해 나가겠다"고 말했다.
한편, SK바이오팜은 기존 중추신경계 질환 신약 외에 항암신약 개발도 적극적으로 진행하고 있다. 교모세포종과 같은 뇌종양을 비롯해 비소세포폐암 등 다양한 암종으로 신약 파이프라인을 확대해 나갈 예정이다.
©(주) 데일리안 무단전재 및 재배포 금지
0
0
기사 공유

이은정 기자 (eu@dailian.co.kr)
기사 모아 보기 >
댓글
0
/ 150
-
최신순
-
찬성순
-
반대순
0 개의 댓글 전체보기
 실시간 랭킹뉴스
실시간 랭킹뉴스
댓글 쓰기